A medida que el flujo de trabajo dental se vuelve cada vez más digital, lo mismo sucede con algunos trámites regulatorios. La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) ha finalizado recientemente una norma que elimina los requisitos que exigían presentar múltiples copias en papel como parte del trámite para la presentación de dispositivos médicos, que a partir de ahora requerirán la presentación de solo un formulario electrónico.
La regulación es en parte una respuesta a una Orden Ejecutiva de 2017 emitida por el presidente Donald Trump, que requiere que los organismos del gobierno estadounidense eliminen dos regulaciones para cada nueva regulación que impongan.
"La FDA está enmendando las regulaciones actuales de dispositivos médicos que requieren la presentación de múltiples copias para mejorar la eficiencia del proceso de revisión al permitir la disponibilidad inmediata de un formulario electrónico para revisión, en lugar de depender únicamente de la versión en papel", declaró la agencia en un documento que especifica los cambios.
"Debido a que un formulario en formato electrónico es fácilmente reproducible, el requisito de presentar copias múltiples (ya sea en formato electrónico o en papel) ya no es necesario", agregó.
Para obtener la aprobación de un dispositivo médico para uso comercial en Estados Unidos, el fabricante debe presentar una notificación previa a la comercialización 510 (k) a la FDA con el objetivo de demostrar que es por lo menos tan seguro y efectivo como un dispositivo médico similar que ya está disponible para su venta en el mercado estadounidense.
Según la Base de datos de Dispositivos Médicos de la FDA, en 2019 recibieron autorización 227 dispositivos dentales.
Dental Tribune habló con H. Kendall Beacham, Vicedecano del Programa de Educación Dental Continua de la Universidad de Nueva York, sobre los ...
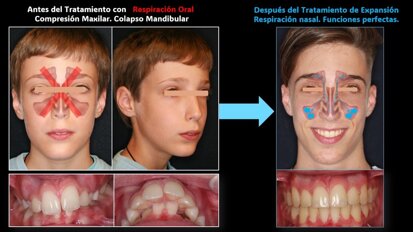
El Dr. Salvador Romero Triana, autor de un capítulo del libro “Odontología en Medicina del Sueño 2”, explica en este artículo la relevancia clínica...
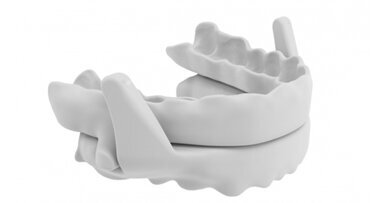
OrthoApnea lanza una nueva generación de dispositivos de avance mandibular (DAM) para el tratamiento conjunto de la apnea del sueño y el desplazamiento ...
El Dr. Pedro A. Cheverez González, ex presidente del Colegio de Cirujanos Dentistas de Puerto Rico y profesor en la Escuela de Medicina Dental de Puerto ...
La Asociación Dental Americana (ADA) invita anualmente a dentistas de todo el mundo a presentar solicitudes para participar como conferencistas en el...
El investigador y conferencista internacional Dr. Armando Hernández Ramírez es una figura reconocida en eventos de todo el mundo. Especialista...
El Dr. Sergio Jiménez y colaboradores de la Universidad Científica del Sur presentaron una innovadora mesa clínica sobre laserterapia ...
La digitalización está cambiando la práctica diaria en las clínicas dentales. Pero, ¿qué papel desempeñan las plataformas en la nube en este cambio....
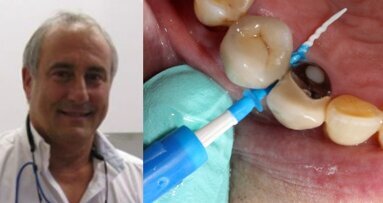
El dentista canadiense Allan Coopersmith ha inventado un dispositivo que facilita la limpieza interdental del biofilm que causa inflamación de las ...
BUENOS AIRES, Argentina — El director clínico de la empresa GO3 Advance, Dr. Jerónimo Tessier, profesor en la Universidad de Buenos ...
Webinars en vivo
lun. 8 de junio 2026
10:00 CST (Mexico City)
Webinars en vivo
lun. 8 de junio 2026
11:00 CST (Mexico City)
Dr. Anthony Mak B.D.S, Prof. Marleen Peumans
Webinars en vivo
lun. 8 de junio 2026
12:00 CST (Mexico City)
Webinars en vivo
mié. 10 de junio 2026
9:00 CST (Mexico City)
Webinars en vivo
mié. 10 de junio 2026
12:00 CST (Mexico City)
Nacho Fernández-Baca DDS, MSc
Webinars en vivo
mié. 10 de junio 2026
17:00 CST (Mexico City)
Webinars en vivo
jue. 11 de junio 2026
11:00 CST (Mexico City)



 Austria / Österreich
Austria / Österreich
 Bosnia y Herzegovina / Босна и Херцеговина
Bosnia y Herzegovina / Босна и Херцеговина
 Bulgaria / България
Bulgaria / България
 Croacia / Hrvatska
Croacia / Hrvatska
 República Checa y Eslovaquia / Česká republika & Slovensko
República Checa y Eslovaquia / Česká republika & Slovensko
 Francia / France
Francia / France
 Alemania / Deutschland
Alemania / Deutschland
 Grecia / ΕΛΛΑΔΑ
Grecia / ΕΛΛΑΔΑ
 Hungría / Hungary
Hungría / Hungary
 Italia / Italia
Italia / Italia
 Países Bajos / Nederland
Países Bajos / Nederland
 Nórdico / Nordic
Nórdico / Nordic
 Polonia / Polska
Polonia / Polska
 Portugal / Portugal
Portugal / Portugal
 Rumania y Moldavia / România & Moldova
Rumania y Moldavia / România & Moldova
 Eslovenia / Slovenija
Eslovenia / Slovenija
 Serbia & Montenegro / Србија и Црна Гора
Serbia & Montenegro / Србија и Црна Гора
 España / España
España / España
 Suiza / Schweiz
Suiza / Schweiz
 Turquía / Türkiye
Turquía / Türkiye
 Reino Unido e Irlanda / UK & Ireland
Reino Unido e Irlanda / UK & Ireland
 Internacional / International
Internacional / International
 Brasil / Brasil
Brasil / Brasil
 Canadá / Canada
Canadá / Canada
 EE UU / USA
EE UU / USA
 China / 中国
China / 中国
 India / भारत गणराज्य
India / भारत गणराज्य
 Paquistán / Pākistān
Paquistán / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 Asean / ASEAN
Asean / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Argelia, Marruecos y Túnez / الجزائر والمغرب وتونس
Argelia, Marruecos y Túnez / الجزائر والمغرب وتونس
 Oriente Medio / Middle East
Oriente Medio / Middle East

















































To post a reply please login or register